近年来,益生菌在生物传感,药物递送和疾病治疗等研究领域的应用前景受到广泛的关注。尤其是在许多结肠相关疾病的治疗中,益生菌通过影响和调节肠道微生物组组成,具有广阔的临床转化潜能。 然而,益生菌的口服递送收到肠道极端环境的影响,导致细菌存活率低和生物利用度低。另一方面,靶标部位炎症及氧化应激的微环境导致益生菌定植抵抗限制了益生菌靶向定植的效率从而降低了治疗的有效性。因此,开发具有高度生物相容性的生物活性物质修饰的益生菌递送平台为解决益生菌治疗局限性提供了新的思路。
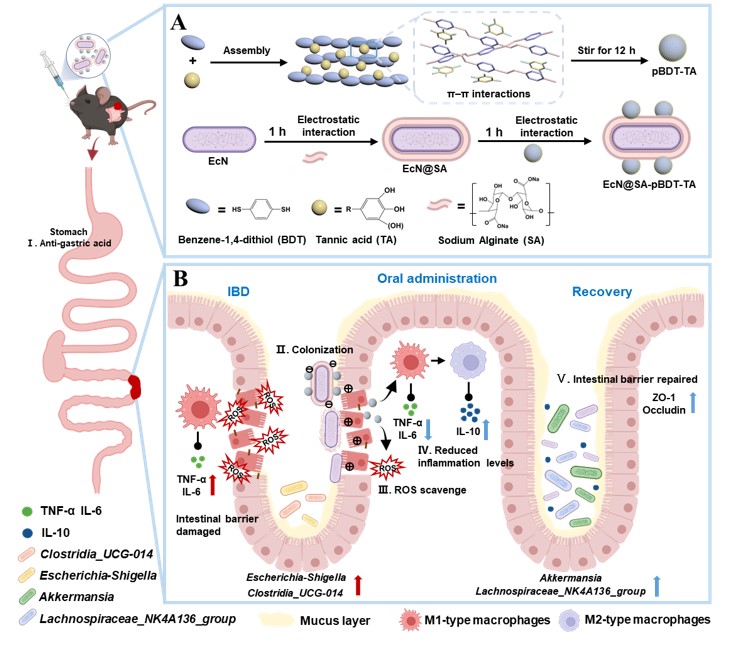
多酚纳米粒子修饰的益生菌用于IBD治疗
多酚是天然生物活性分子,在大自然中种类丰富,能够调节氧化损伤和炎症应激免疫反应。多酚自组装纳米材料作为一种新型的功能纳米材料,具有良好的生物活性和较高的生物安全性。本研究基于单宁酸(Tannin acid, TA)独特结构的启发,利用自聚合芳香族二巯基(BDT)和TA自组装制备了纳米结构的pBDT-TA。通过多酚纳米粒和海藻酸钠(SA)层层组装包被益生菌,为益生菌肠道递送提供了重要的保护作用。炎症性肠病(Inflammatory bowel diseases,IBD)是发生在胃肠道的慢性炎症疾病,其发病机制通常伴随着活性氧(ROS)水平的升高、肠道免疫和微生物稳态失衡。在过去的十年里,IBD病例的空前增加给全球公共医疗系统带来了巨大的财政负担。肠道菌群失衡是IBD的一个重要标志,大肠杆菌Nissle 1917(EcN)是一种商业化的益生菌,它可以通过改善结肠内的细菌多样性影响IBD的治疗效果。该课题利用多酚纳米粒搭载EcN构建协同治疗体系,能够通过调节氧化还原平衡、减轻炎症和重塑肠道微生物群来促进肠道稳态有效预防和治疗IBD。
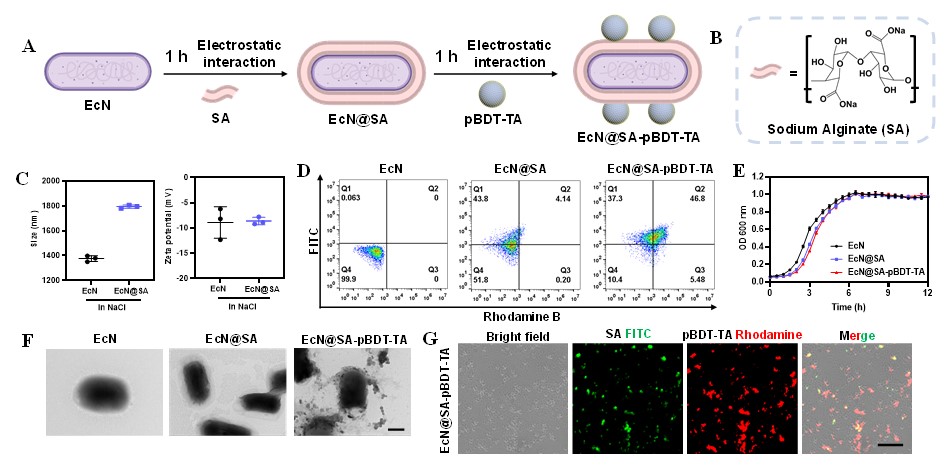
多酚纳米粒修饰益生菌的制备及表征
该论文通过分子间的π-π相互作用制备了表面光滑、尺寸均一且稳定性良好的pBDT-TA纳米球。pBDT-TA纳米球在细胞水平表现出良好的生物相容性和细胞摄取能力,能够清除胞内ROS,保护细胞免受H2O2刺激带来的氧化损伤,并下调炎性免疫激活水平,这表明IBD是一个优良的IBD微环境调控的候选者。通过静电相互作用,将SA和多酚纳米球层层包被在EcN的表面,利用荧光显微镜,流式细胞仪和透射电镜证实SA和多酚纳米球能够成功包被在EcN的表面,形成保护层,有效缓解IBD肠道中氧化损伤的环境并重塑促炎微环境,提高了益生菌在炎症部位的靶向富集。DSS诱导小鼠结肠炎模型中也进一步证实,该协同治疗体系能够提高了益生菌的口服生物利用度,改善DSS诱导的小鼠结肠炎的相关指标。
本研究设计构建了多酚纳米粒载药体系修饰的益生菌在小分子抗炎药物递送和炎症性肠病微环境重塑方面具有巨大的潜力和良好的应用前景,为协同治疗IBD提供了新的方向。相关研究成果以“Polyphenolic nanoparticles modified probiotics for microenvironment remodeling and targeted therapy of inflammatory bowel disease”为题,于2024年5月10日发表在纳米科学领域TOP期刊《ACS Nano》(IF 17.1)上。
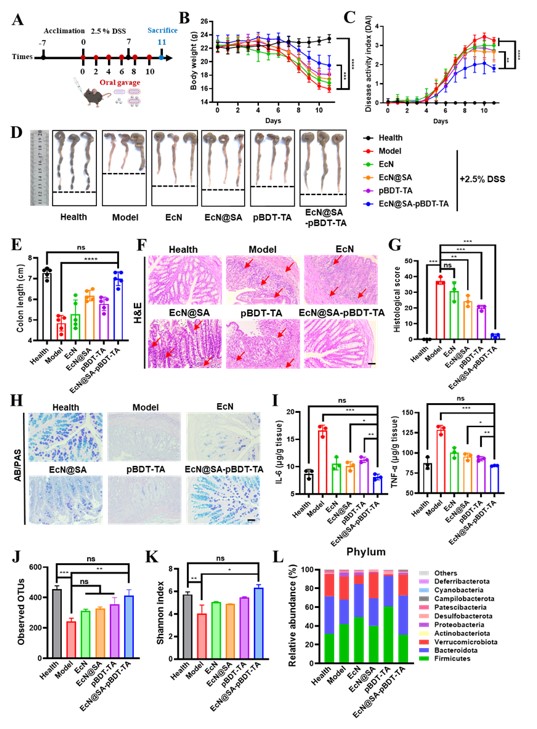
EcN@SA-pBDT-TA可改善DSS诱导的小鼠结肠炎
该研究得到了国家自然科学基金项目的支持(42277279)和浙江省自然科学基金资助项目支持(LY21E030011)。浙江工业大学靳远祥教授为该论文的通讯作者,浙江工业大学胡青莲副教授为论文第一作者,2021级硕士研究生李婧瑜为本课题做出了贡献。
论文信息:Qinglian Hu, Jingyu Li, Tong Wang, Xiangchi Xu, Yuxuan Duan, Yuanxiang Jin*,Polyphenolic Nanoparticles Modified Probiotics for Microenvironment Remodeling and Targeted Therapy of Inflammatory Bowel Disease. ACS NANO, 2024
论文链接:https://doi.org/10.1021/acsnano.4c00830

